
- Главная
- Библиотека
- Научные статьи
- Модель комплементарного взаимодействия коротких пептидов с двойной спиралью ДНК
Модель комплементарного взаимодействия коротких пептидов с двойной спиралью ДНК
Сравнение пространственного расположения функциональных групп нуклеиновых оснований на поверхности большой канавки двухспиральной ДНК и функциональных групп коротких пептидов показывает, что эти полиамфолитные структуры имеют возможность многоточечного комплементарного взаимодействия. В качестве примера представлена модель комплементарного связывания синтетического тетрапептида эпифиза Ala-
Как известно, нормальная клетка отвечает на внешние или внутренние изменения изменением интенсивности транскрипции активных генов и синтеза РНК, Одним из факторов патологического состояния организма является замедление этих процессов, в частности, нарушение процессов инициирования транскрипции [12]. В то же время появились сообщения о том, что некоторые белки, контролирующие клеточный цикл, могут быть активны как факторы транскрипции [16].
Вопрос о механизме инициирования транскрипции решается исследованием структур факторов транскрипции и определением их сайтов связывания с двойной спиралью ДНК на промоутерном (некодирующем) участке гена. Со времени появления первых работ в этой области в начале
Тогда казалось, что специфическая активность многих высокомолекулярных факторов транскрипции локализована на сравнительно коротких участках пептидной цепи, состоящих из 30–100 аминокислотных остатков [31]. Эти наблюдения выделили новую проблему фармакологии и медицины. Требовалось определить, какова минимальная длина и аминокислотная последовательность короткого пептида, непосредственно и селективно контактирующего с промоутерным участком гена и способного имитировать действие фактора транскрипции. Более подробно молекулярные механизмы инициирования транскрипции в клетках представлены в монографии [27. Р. 341–403].
Обычный подход к отысканию сайта связывания в структуре белка состоит в использовании иммуноспецифических методов. Так, например, был определен участок
В то же время были выделены и исследованы эндогенные регуляторные пептиды человека, которые проявляли тканеспецифическую активность при использовании в сверхмалых концентрациях. Исследование продуктов гидролиза гемоглобина и пептидов, содержащихся в питательной среде при культивировании человеческих эритроцитов, показало, что короткие отрезки цепей глобинов проявляют активность, несвойственную исходному гемоглобину: они связываются с опиатными рецепторами, потенцируют действие брадикинина [24]. Регуляторные пептиды были также выделены из живой культуры клеток костного мозга, исследованы в отношении специфической регуляторной активности и названы миелопептидами [6].
Эксперименты последних лет показали, что как природные пептидные препараты, так и их синтетические аналоги — тетрапептиды определенной структуры — проявляют тканеспецифическую активность, участвуя в активации хроматина и нормализуя ритм белкового синтеза в культуре тканей [1, 4, 5, 9] и на уровне целого организма [10, 13, 26, 32]. Можно предполагать, что короткие пептиды, поддерживающие аутокринную регуляцию, являются миметикамн и агонистами высокомолекулярных факторов транскрипции.
Механизмы проникновения коротких пептидов в клетку и в клеточное ядро могут быть различны. По мнению
Современные представления о проницаемости цитоплазматической и ядерной мембран показывают, что для проникновения через эти мембраны существуют и диффузионные пути.
Кроме известных ранее ионных каналов и процессов пиноцитоза, были открыты каналы, образованные семейством трансмембранных белков поринов, присутствующих в митохондриальной и цитоплазматической мембранах [25]. Эти белки имеют в своем составе до 50% гидрофильных аминокислот и структурные мотивы амфифильной
Семейство поринов включает подсемейство аквапоринов — белков, контролирующих потоки воды в клетку и из клетки в зависимости от небольших изменений рН внешней среды [17].
Мембраны ядра также имеют развитую систему транспортных пор, образованных белковыми комплексами- нуклеопоринами, которые контролируют транспорт нуклеопротеиновых комплексов в ядро и из ядра [33]. Внутренний диаметр нуклеопор имеет порядок 42 н.м, так что они проницаемы для диффундирующих молекул с молекулярной массой до 5000 Да [27. Р, 69].
Таким образом, возможность проникновения коротких пептидов в клетку и в клеточное ядро не вызывает принципиальных сомнений. Наши экспериментальные исследования согласуются с представлениями о проникновении коротких пептидов в клетку и ее ядро, так как после добавления пептида в культуру клеток выявлены изменения в состоянии хроматина, В работах [1, 8, 13] на клетках в культуре тканей было доказано, что короткие синтетические пептиды не только проникают в клетку через цитоплазматическую и ядерную мембраны, но и участвуют в активации отдельных генов, в частности гена теломеразы [5].
В работе [9] было исследовано воздействие коротких синтетических пептидов на изменения гетерохроматина в лейкоцитах и обнаружена активация рибосомных генов, деконденсация плотно упакованных фибрилл хроматина и высвобождение генов, репрессированных в результате возрастной конденсации эухроматиновых районов клеток.
Однако до настоящего времени существует очевидный разрыв между многочисленными наблюдениями регуляторных воздействий нейрогормонов и синтетических олигопептидов на состояние хроматина и представлениями о молекулярных механизмах селективного связывания этих пептидов с промоутерными участками генов.
Среди коротких синтетических пептидов, исследованных нами ранее в отношении активации хроматина, наибольшую эффективность проявил синтетический тетрапептид эпифиза (Ala-
Основы комплементарных взаимодействий в системе «Олигопептид — олигонуклеотид»
Цель нашей работы состояла в отыскании возможного механизма селективного узнавания и связывания коротких пептидов с той частью генетического аппарата, которая ответственна за инициирование белкового синтеза.
Механизм узнавания в системе «пептид — ДНК» по принципу «одна аминокислота — одна пара нуклеотидов» не может быть специфическим [14]. Из 20 аминокислот по крайней мере 8 могут связываться одновременно с функциональными группами двух соседних пар оснований, так как имеют достаточно длинные и подвижные боковые функциональные группы. Однако селективность такого связывания невелика. Аминокислоты с ароматическими боковыми группами могут связываться с двойной спиралью ДНК в результате взаимодействия ароматических колец аминокислот и нуклеотидов [5, 20].
Более высокая селективность (избирательность) узнавания и связывания обеспечивается кооперативным многоточечным взаимодействием в системе «олигопептид — олигонуклеотид».
Молекулярное узнавание в биологии основано на точном соответствии молекулярных поверхностей взаимодействующих молекул и совпадении метрических параметров расположения на этой поверхности взаимодействующих функциональных групп [39]. Структурное соответствие такого рода называется матричной комплементарностью.
Пептидная цепь, состоящая из
При построении модели матричной комплементарности тетрапептида с соответствующим участком двойной спирали ДНК использованы литературные данные о геометрических характеристиках двойной спирали ДНК и пептидной цепи [5, 38, 7] и о закономерностях полифункционального взаимодействия ДНК с полиамфолитами [3, 18].
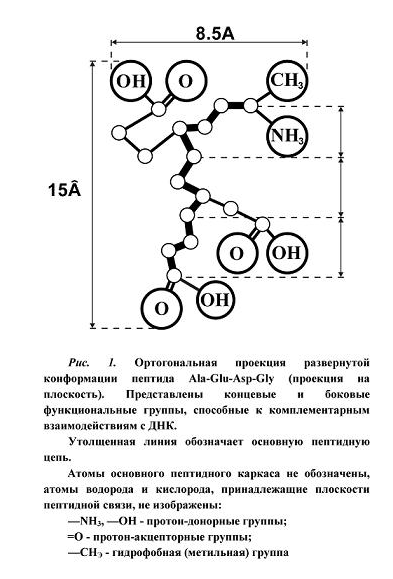
В конкретном случае при исследовании конформационных особенностей тетрапептида Ala-
Нуклеотидные пары двойной спирали ДНК в активном хроматине располагаются друг над другом в почти параллельных плоскостях. На один оборот невозмущенной двойной спирали ДНК приходится 10 пар оснований; среднее расстояние между плоскостями пар оснований составляет 3.4, А [5]. Известно, что фосфодиэфирные каркасные цепи разделяют поперечное сечение двойной спирали ДНК на два неравных участка. В связи с этим на молекулярной поверхности двойной спирали различают большую и малую канавки шириной 22.2 и 11.8, А соответственно, разделенные двумя фосфодиэфирными цепями [12, 38].
На рисунке представлена ортогональная проекция на плоскость страницы
Таким образом, двойная спираль ДНК и пептидная цепь имеют определенное метрическое соответствие: длина пептидной цепи в
При поиске последовательности нуклеотидных пар, комплементарной этому тетрапептиду по расположению
Большинство промоутерных (некодирующих) участков генов содержат в цепях многочисленные повторения сравнительно коротких последовательностей (нуклеотидных блоков). Длина таких блоков обычно составляет 6–10 пар оснований (п. о.),
Метрические характеристики расположения функциональных групп отдельных нуклеотидных пар, которые оказываются на поверхности большой канавки двойной спирали ДНК при объединении нуклеотидных пар в общую структуру определяют потенциал молекулярной поверхности большой канавки [39]. Очевидно, что каждая последовательность нуклеотидных пар экспонирует на поверхность большой канавки ДНК собственный уникальный орнамент функциональных групп. Эти группы могут участвовать в водородных, ионных связях и в гидрофобных взаимодействиях с пептидной цепью, если расположение боковых групп пептида комплементарно соответствует этому орнаменту.
Модель комплементарного взаимодействия тетрапептида Ala-GIu-Asp-Gly (AEDG) с двойной спиралью ДНК
Для наших исследований мы выбрали семейство высокомолекулярных факторов транскрипции, имеющих характерный мотив «спираль — петля — спираль», структуры которых подробно изучены [14, 31, 34]. Многие из них участвуют в инициировании транскрипции жизненно важных генов: теломеразы и РНК полимеразы II [30, 31, 40, 41]. Известно, что участок петли этих белков состоит из 14 остатков, в основном, аспарагиновой, глутаминовой аминокислот и треонина [27. Р. 59]. Исследуемый нами синтетический пептид качественно подобен этой петле по соотношению гидрофильных и гидрофобных групп.
Межмолекулярные взаимодействия между пептидом AEDG и ДНК осуществляются в виде водородных связей между функциональными группами обоих участников. Длина водородной связи в таких системах обычно равняется 2.0–2.5, А,
При построении модели комплементарных межмолекулярных связей тетрапептида с ДНК учитывалась длина ковалентных связей 1.5, А,
На рисунке представлена ортогональная проекция этого пептида, комплементарно совмещенного с последовательностью нуклеотидных пар двойной спирали ДНК. Показано, как тетрапептид AEDG расположен в большой канавке двойной спирали ДНК в соответствии с требованием комплементарности функциональных групп этого тетрапептида функциональным группам нуклеотидных пар. Отличительной особенностью предлагаемой модели является то обстоятельство, что пептид в большой канавке взаимодействует одновременно с функциональными группами оснований обеих цепей двухспиральной ДНК.
Следует отметить, что сходная метрика расположения функциональных групп на поверхности большой канавки двойной спирали для нуклеотидных пар, А — Т и G — С, высокая подвижность функциональных групп концевых аминокислотных остатков аланина и глицина, а также вариабельность угла наклона плоскости нуклеотидных пар по отношению к оси двойной спирали ДНК позволяют тетрапептиду AEDG связываться комплементарно с последовательностями ATTTG, GTTTC, СТТТС. хотя прочность этих связей будет слабее, чем с АТТТС.
Как уже указывалось, тетрапептид AEDG представляет особый интерес именно
Специфический ген, расположенный в субтеломерной области, также содержит блок АТТТС в составе своего промоутерного участка и может служить сайтом связывания синтетического тетрапептида эпифиза [28].
Одной из причин старения организма является замедление синтеза белка. Транскрипция всех белковых генов осуществляется ферментом
В текущей литературе можно обнаружить значительное количество публикаций о регуляторном действии коротких пептидов [37, 43]. Разница между высокомолекулярными факторами транскрипции и короткими пептидами, участвующими в инициировании транскрипции генов, проявляется, прежде всего, в процессах транспорта этих молекул из внешней среды в ядро клетки. Кроме того, короткие пептиды тканеспецифичны, но не видоспецифичны и не проявляют иммуногенности.
Предлагаемая нами молекулярная модель взаимодействия коротких пептидов с двойной спиралью ДНК на промоутерном участке гена заслуживает экспериментальной проверки на уровне
Выводы. Структуры пептидов и двойной спирали ДНК обеспечивают условия для узнавания и комплементарного связывания пептида с определенной последовательностью функциональных групп нуклеотидов на поверхности большой канавки двойной спирали ДНК в области промоутерного участка гена. В связывания участвуют обе цепи двойной спирали ДНК. Предложенный метод молекулярного моделирования комплементарного связывания пептида на промоутерном участке гена может быть полезен для нахождения потенциально активных коротких пептидов — миметиков факторов транскрипции — по данным о последовательности нуклеотидов на промоутерном участке целевого гена.
Хавинсон В.Х., Шатаева
Литература
1. Анисимов С.В., Бохелер К.Р., Хавинсон В.X, Анисимов
2. Ашмарин И.П., Каразеева
3. Биологически активные вещества в растворах / Под ред. академика
4. Бродский В.Я., Хавинсон В.X., Золотарев Ю.А. и др. Ритм синтеза белка в культурах гепатоцитов крыс разного возраста. Норма и действие пептида ливагена // Изв. АН. Серия биология. 2001. № 5. С. 517–521.
5. Зенгер В. Принципы структурной организации нуклеиновых кислот. М.: Мир, 1987. 584 с.
6. Петров Р.В., Михайлова А.А., Фомина Л.А., Степаненко
7. Попов
8. Хавинсон В.X., Бондарев И.Э., Бутюгов
9. Хавинсон В.X., Лежава Т.А., Малинин
10. Хавинсон
11. Шатаева U.K., Ряднова И.Ю., Хавинсон В.X Исследование информационной ценности олигопептидных блоков в регуляторных пептидах и белках // Успехи совр, биологии, 2002. Т. 122. № 3. С. 281–288.
12. Alberts В., Bray D., Lewis J., Raff M., Roberts К., Watson
13. Anisimov S.
14. Atchley W.R., Wallenberg К.R., Fitch W.M., Terhalle W., Dress
15. Blasco
16. Dynlacht B.D., Regulation of transcription by proteins, that control the cell cycle // Nature. 1997. Vol. 389. P. 149–152.
17. Echevarria M., Ilundain A, A, Aquaporins // J. Physiol. Biochem, 1998. Vol. 54. № 2. P. 107–118.
18. Gallagher K., Sharp K. Electrostatic contributions to heat capacity changes of
19. Graf J., Ogle R.C., Robey F.A. et al. Pentapeptide from the laminin Bl chain mediates cell adhesion and binds the 67 000 Laminin receptor // Biochemistry. 1987. Vol. 26. № 22. P. 6896–6900.
20. Gromiha M., Santhosh C., Suwa M. Influence of
21. Harley С.В., Futcher А.В., Greider
22. Harrison S.C. A structural taxonomy of
23.
24. Ivanov V.Т., Karelin A.A., Philippova M.M. et al. Hemoglobin as a source of endogenous
25. Kayser H., Kratzin Y.D. et al. Identification of human porins, II Characterisation and primary structure of a
26. Khavinson
27. Lodish H., Berk A., Zipursky S.L» Matsudaira P., Baltimore D., Darnell J. Molecular cell biology / Library of Congress
28. Mah N., Stoehr H., Schulz H.L., White A., Weber
29. Matsumura S., Takakashi Т., Ueno A., MiPiara Н. Complementary nucleobase interaction enhances
30. Mita K., Tsuji H., Morimyo M., Takahashi E., Nenoi M., Ichimura S., Yamauchi M., Hongo E., Hayashi A. The human gene encoding the largest subunit of RNA polymerase II // Gene. 1995. Vol. 159. № 2. P. 285–286.
31. Mitchell P.J., Tijan R. TranscriptionaJ regulation in mammalian cells by
32. Morozov
33. Ohno M., Fornered M., Mattaj
34. Pabo C.O., Sauer
35. Parkinson G., Wilson C., Gunasekera A., Ebright Y.W., Ebright R.E., Bermcm
36. Rentzeperis D., Мотку
37. Ryu S., Zhou S., Ladurner A.G., Tjian R. The transcriptional cofactor complex CRSP is required for activity of the
38. Van Holde
39. Wainer P.K., Langridge R., Blaney J.M., Kollman
40. Wick
41. Woychik N.A., Hampsey M. The RNA polymerase II machinery: structure illuminates function // Cell. 2002. Vol. 108. P. 453–63.
42. Wrighton N.C., Farretl F.X. et al, Stnal I peptides as potent mimetics of the protein hormone Erytropoietin // Science. 1996. Vol. 273. July. P. 458–163.
43. Yang W., Van Duyne
в курсе акций и новинок